

成熟的临床研究产品体系
临床试验信息管理系统CTMS
应用于多中心临床试验规范化管理的专业软件,对整个临床试验各个阶段的进度、人员、沟通、文档等进行管理和控制。
电子数据采集系统EDC
用于药物临床试验数据的采集、监察、检索、管理、质控以及统计。
交互式网络应答系统IWRS
用于临床试验中随机化分配、受试者管理、药品管理等,可用于多中心和跨国的临床试验。


数据管理和统计分析
智能一键式建库
采用sasmeta文件,上传EDC系统,实现快速准确率100%建库,减少80%测试的工作量。
SAS自动化系统
自动化SDTM制作,自动化TFLs生成,自动化define。
CDISC标准实施
用最小的成本将所有项目均实施CDISC标准,为客户项目合并分析提供简洁的数据处理工作。


医学事务
药物警戒服务
个例安全性报告、SOP撰写、PV相关文件撰写、文献检索。
临床试验文件撰写
临床试验方案撰写、研究病历、研究者手册、总结报告撰写。首次人体剂量估算、采血点设计、给药设计等。
医学支持
从医学角度分析临床试验过程中出现的医学问题。

临床、非临床数据转化
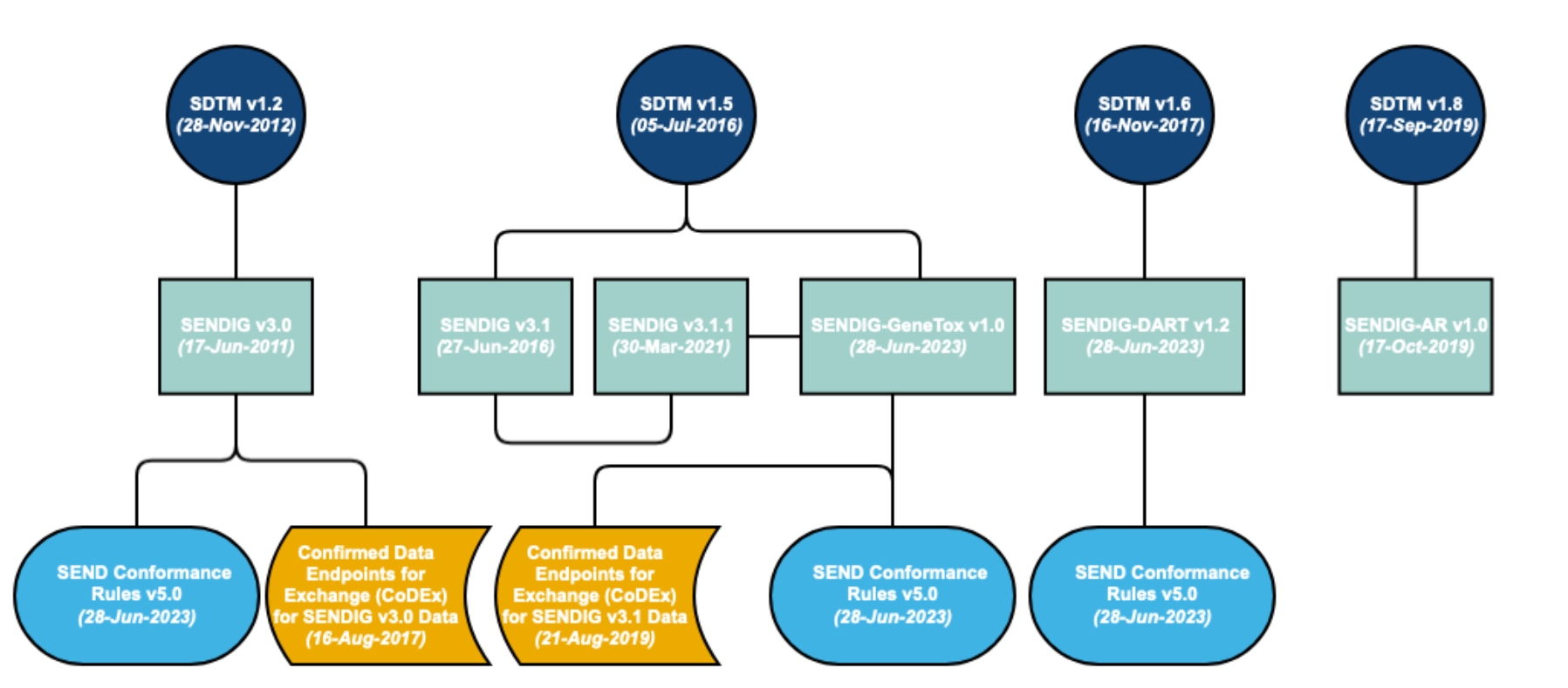
SEND转化
目前CDISC标准已被欧、美、日等药监部门接受,广泛应用于临床研究中,洛必塔为中国本土少有的可以提供SEND转换服务之一的公司。
SDTM转化
SDTM转化服务旨在帮助生物制药行业的企业将临床试验数据转化为标准化数据模型(SDTM),这是向美国食品药品监督管理局(FDA)等监管机构提交数据的国际标准格式。此服务包括从原始数据到SDTM格式的转换,确保数据符合监管要求,同时提高数据的整理效率和质量。


定量药理学
群体药代动力学PopPK
Pop PK模型优化给药方案,用于FDA注册或科研文章发表。
PBPK生理药代动力学
生理药物动力学(Physiologically-based pharmacokinetics,PBPK)是一种以系列数学方程式整合药物的理化性质、机体真实的生理生化性质和解剖学结构等信息,以表征药物通过血液循环系统在不同器官和组织中分布、转运和消除(代谢和排泄)过程,从而实现预测药物体内(如血浆和组织等)动力学过程(吸收、分布、代谢和排泄,ADME)的整体(Whole body)模型。

